
6月25日华东理工大学刘昌胜院士和王靖教授课题组在Advanced Science期刊上发表了题为“Sulfated Polysaccharide Regulates the Homing of HSPCs in a BMP-2-Triggered In Vivo Osteo-Organoid”,介绍了一类磺化多糖能够调控造血干细胞(HSPCs)在体类骨器官中的归巢行为,实现HSPCs丰度与功能的有效提升,为干细胞移植方案提供了新的前景。
造血干细胞移植(HSCT)是目前治疗包括恶性血液病等多种疾病的首选方案,但造血干细胞(HSPCs)的来源及数量不足制约着相关治疗的实施。骨髓作为HSPCs的“蓄水池”,是HSPCs的主要来源。此前,华东理工大学刘昌胜院士和王靖教授课题组基于“材料生物学”概念,利用活性生物材料,开发出一种骨形态发生蛋白-2(BMP-2)启动的在体类骨器官(in vivo osteo-organoid)。该类骨器官含有多种治疗性细胞,包括HSPCs,有望为多种疾病治疗提供一种HSPCs的全新来源。
在此基础上,该课题组进一步发现一类磺化多糖能够调控HSPCs于在体类骨器官中的归巢行为,实现HSPCs丰度与功能的有效提升。
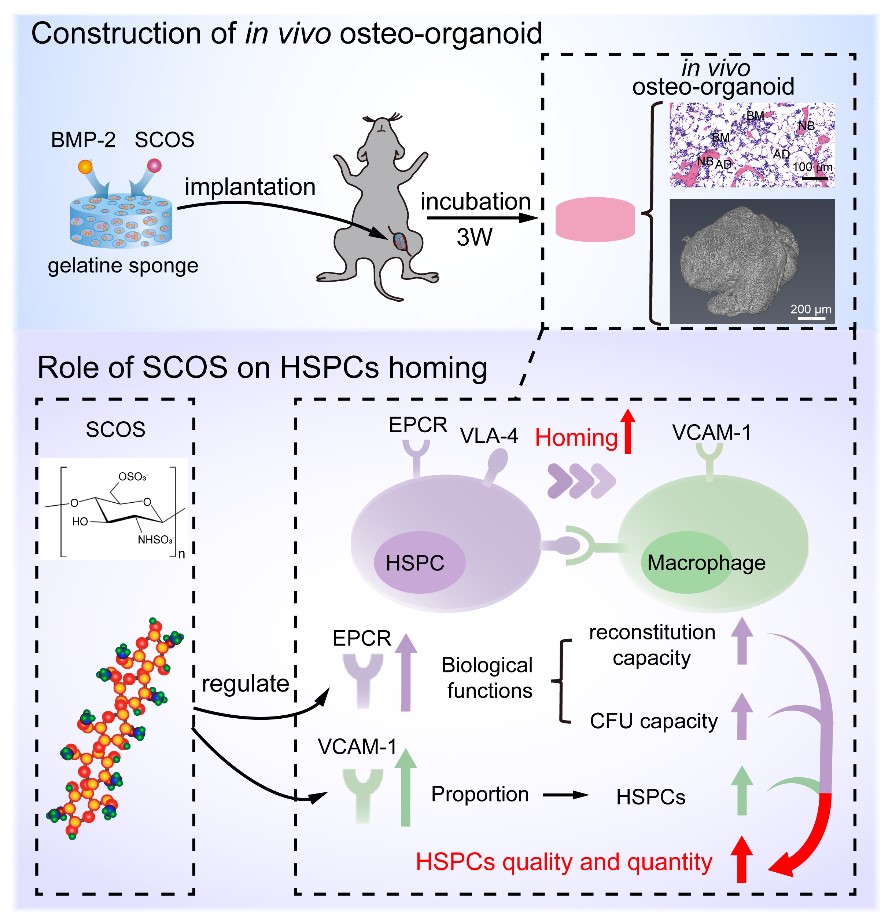
图1. 磺化壳寡糖(SCOS)提高在体类骨器官中HSPCs的归巢及造血重建能力。
作者通过系统研究了两种不同分子量的壳聚糖磺化产物,即磺化壳聚糖(SCS)与SCOS。其中两种壳聚糖磺化产物的添加都能够有效提升在体类骨器官的相对骨体积,但对皮质骨的厚度没有影响。进一步的功能性实验证实,SCOS能够提高在体类骨器官中HSPCs的集落形成能力及造血重建能力,尤其是淋巴细胞的重建水平。同时流式细胞术检测证实,SCOS能够提高在体类骨器官中HSPCs的相对丰度,而这种提高是通过巨噬细胞介导的VCAM-1/VLA-4信号轴实现。
综上所述,该研究系统研究了壳聚糖磺化产物在HSPCs调控中的新功能,为后续进一步优化基于在体类骨器官系统的细胞治疗策略提供新思路。
设施贡献
用户使用动物系统RS-2000 X射线辐照仪致死剂量辐照小鼠,后续移植细胞,并利用复合激光显微镜系统流式细胞仪LSRFortessa 分析移植后造血重建嵌合水平。国家蛋白质科学研究(上海)设施为该课题研究评价造血干细胞功能提供重要支持,证明了该课题所研究SCOS具有提高干细胞重建能力的现象。